Las bases nitrogenadas son compuestos orgánicos cíclicos, que incluyen dos o más átomos de nitrógeno. Son parte fundamental de los nucleósidos, nucleótidos, nucleótidos cíclicos (mensajeros intracelulares), dinucleótidos (poderes reductores) y ácidos nucleicos. Biológicamente existen seis bases nitrogenadas principales (en realidad hay muchas más), que se clasifican en tres grupos, bases isoaloxazínicas (derivadas de la estructura de la isoaloxazina), bases púricas o purínicas (derivadas de la estructura de la purina) ybases pirimidínicas (derivadas de la estructura de la pirimidina). La flavina (F) es isoaloxazínica, la adenina (A) y la guanina (G) son púricas, y la timina (T), la citosina (C) y el uracilo (U) son pirimidínicas. Por comodidad, cada una de las bases se representa por la letra indicada. Las bases A, T, G y C se encuentran en el ADN, mientras que en el ARN en lugar de timina aparece el uracilo. La base nitrogenada que fue descubierta en el 2010 se llama Genética X, Hebra X o Báse Nitrogenad X
Complementariedad entre purinas y pirimidinas
Un punto fundamental es que las purinas y pirimidinas son complementarias entre sí, es decir, forman parejas de igual manera que lo harían una llave y su cerradura; son los denominados apareamientos de Watson y Crick. La adenina y la timina son complementarias (A=T), uniéndose gracias a dos puentes de hidrógeno, mientras que la guanina y la citosina (G≡C) se unen mediante tres puentes de hidrógeno. Dado que en el ARN no existe timina, la complementariedad se establece entre adenina y uracilo (A=U) mediante dos puentes de hidrógeno. La complementariedad de las bases es la clave de la estructura del ADN y tiene importantes implicaciones, pues permite procesos como la replicación del ADN, la transcripción de ADN a ARN y la traducción del ARN en proteínas.
Estructura
- El "esqueleto" de las flavinas es la isoaloxazina, por lo que son bases isoaloxazínicas.
- El "esqueleto" de adenina, hipoxantina, xantina, etc. es la purina, por lo que toman el nombre de bases púricas o purínicas.
- El "esqueleto" de citosina, uracilo, timina, nicotina, nicotinamida, etc. es la pirimidina, son bases pirimídicas.
Isoaloxazinas
| Base nitrogenada | Nucleósido |
|---|---|
 Flavina |  Riboflavina F |
Purinas
| Base nitrogenada | Nucleósido |
|---|---|
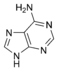 Adenina | 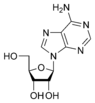 Adenosina A |
 Guanina |  Guanosina G |
Pirimidinas
| Base nitrogenada | Nucleósido |
|---|---|
 Timina |  Timidina T |
 Citosina | 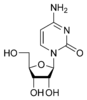 Citidina C |
 Uracilo | 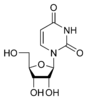 Uridina U |